درسنامه علوم نهم فصل اول
آموزش کامل فصل اول علوم نهم – مواد و نقش آنها در زندگی
درسنامه فصل اول علوم نهم به همراه پاسخ کامل تمامی فعالیت های متن کتاب

![]()

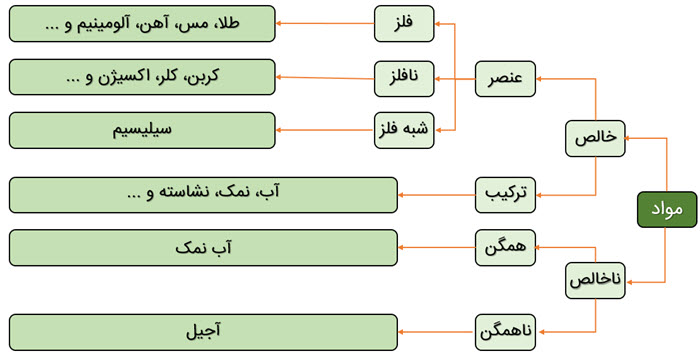
در علوم هفتم با این طبقه بندی نیز آشنا شدید:
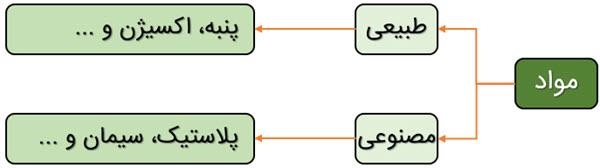
برخی از مواد مانند منیزیم، آهن، طلا، مس، نقره و … فلز هستند و کاربردهای بسیاری مانند خانه سازی، پل سازی، ابزار، زیورآلات، حمل و نقل و … دارند و برخی دیگر مانند چدن، فولاد، برنج و … که نوعی آلیاژ هم هستند؛ از فلز ساخته شده اند.

تصویر برخی وسایل ساخته شده از فلزها

آلیاژ چیست؟ به مخلوطی از دو یا چند فلز باهم یا فلز با نافلز آلیاژ گفته می شود. مثل فولاد، چدن، برنج و …
در سال گذشته با برخی از خواص آهن، آلومینیم و طلا آشنا شدیم. امسال نیز با خواص فلزهای دیگری آشنا خواهیم شد.
ویژگی ها و کاربردهای مس :
- از طریق ذوب سنگ معدن در دمای بالا به دست می آید.
- فلزی براق و سرخ رنگ است.
- فلزی با رسانایی الکتریکی زیاد است.
- مقاومت بالایی در برابر خوردگی دارد.
- قابلیت مفتول شدن دارد.
- از ظروف مسی برای پختن غذا و سیم های مسی در سیم کشی ساختمان استفاده می شود.
ویژگی های دیگر فلز مس که در کتاب به آن اشاره نشده :
- اولین فلز استخراج شده از سنگ معدن است.
- نماد شیمایی آن Cu و عدد اتمی آن 29 است.
- از آلومینیم و آهن سنگین تر و از طلا سبک تر است.
- در تهیۀ آلیاژهایی مانند برنج و برنز کاربرد دارد.
- در ساختار بعضی ترکیبات شیمایی مانند کات کبود (مس سولفات، CuSO4) به کار رفته است.

ترتیب واکنش پذیری فلزهای مس، آهن و منیزیم با اکسیژن عبارتند از: ![]()
- آهن با اکسیژن به کندی واکنش می دهد و به زنگ آهن تبدیل می شود.
- فلز مس نیز با اکسیژن به کندی ترکیب و به مس اکسید تبدیل می شود.
- اگر یک تکه نوار منیزیم را روی شعلۀ چراغ بگیرید، به سرعت می سوزد و نور خیره کننده ای تولید می کند.
- طلا برخلاف این سه فلز با اکسیژن ترکیب نمی شود.
معادلۀ نوشتاری واکنش این فلزات با اکسیژن بصورت زیر است:
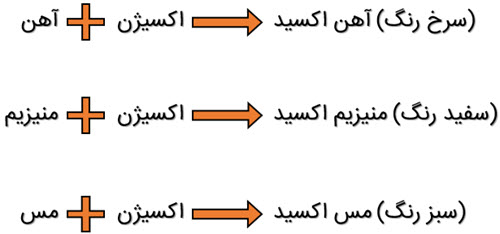
![]()
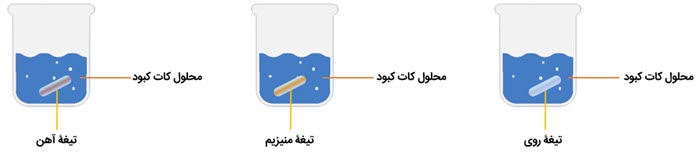
سه بشر هم اندازه را شماره گذاری می کنیم و درون هر یک تا یک سوم حجم آن، آب می ریزیم.
یک قاشق چای خوری کات کبود در هر یک از بشرها حل می کنیم.
در بشر شمارۀ (1) تیغۀ آهن، در بشر شمارۀ (2) تیغۀ منیزیم و در بشر شمارۀ (3) تیغۀ روی قرار می دهیم.
بعد از مدتی مشاهده می کنیم رنگ فلز منیزیم داخل محلول کات کبود به سرعت تغییر رنگ داده و یک لایه مس روی آن می نشیند، سپس فلز روی داخل محلول و در نهایت فلز آهن تغییر رنگ می دهد.
بر این اساس می توان سرعت واکنش پذیری این سه فلز را به صورت زیر ترسیم کرد.
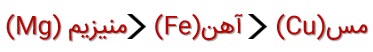

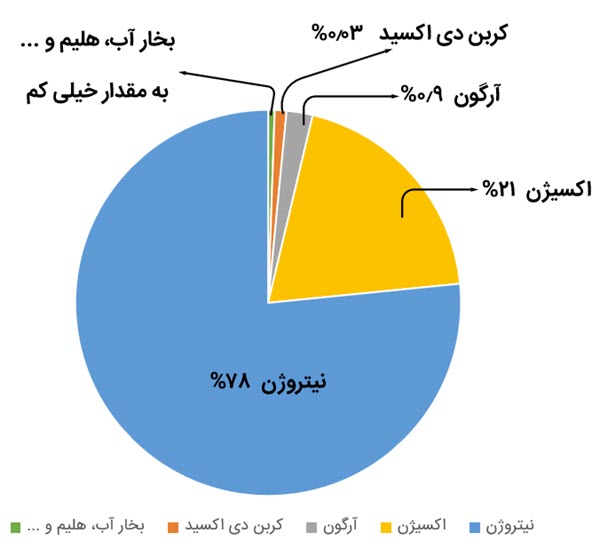
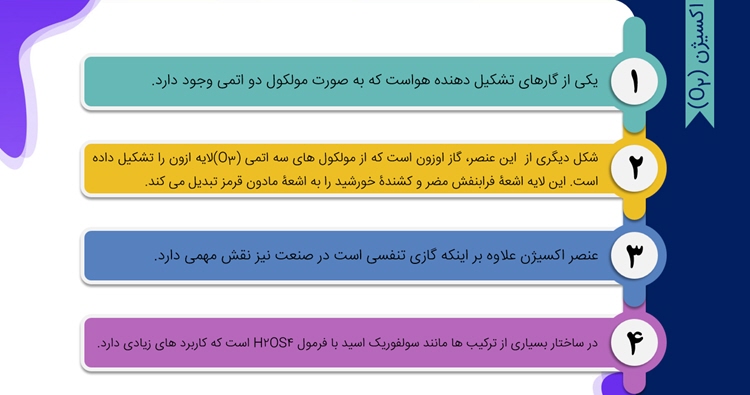
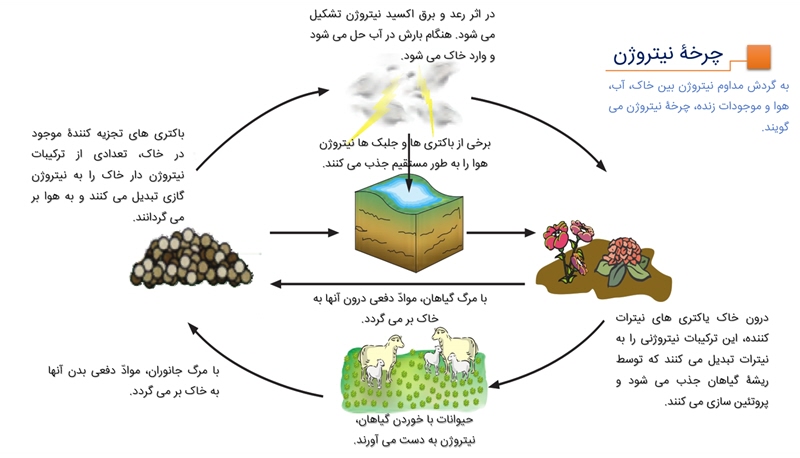
در علوم هشتم آموختیم : هوای پاک یک مخلوط گازی و همگن است.
مهم ترین اجزای تشکیل دهندۀ هوا، گازهای نیتروژن، اکسیژن، آرگون، کربن دی اکسید و بخار آب است.


نام ترکیب سولفوریک اسید
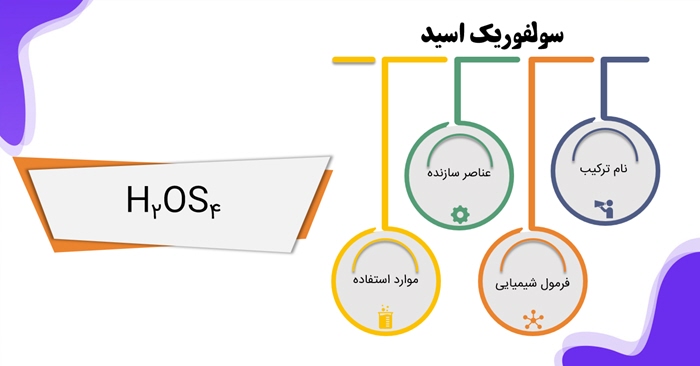
فرمول شیمایی سولفوریک اسید
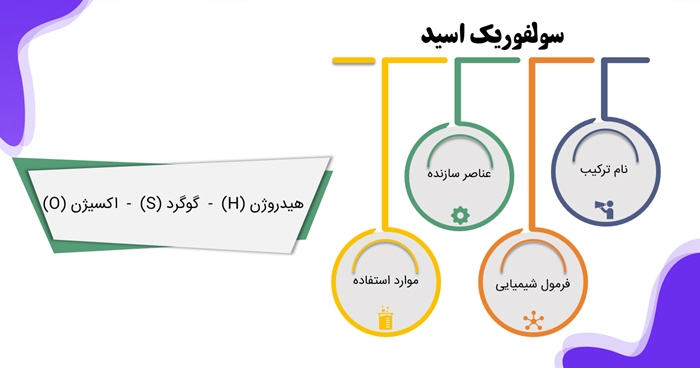
عناصر سازنده سولفوریک اسید
هیدروژن : هیدروژن یا آبزا (به انگلیسی: (Hydrogen، با نماد شیمیایی H) نام یک عنصر شیمیایی در جدول تناوبی با عدد اتمی ۱ است. هیدروژن سبکترین عنصر در جهان است و بیش از دیگر عنصرها میتوان آن را به صورت آزاد در طبیعت پیدا کرد. میتوان گفت نزدیک به ۷۵٪ از جرم جهان از هیدروژن ساخته شده است.
گوگرد : گوگرد با نماد شیمیایی S و عدد اتمی 16 ، یه صورت جامدی زرد رنگ در ترکیب سنگ های مناطق آتش فشانی و در اطراف دهانۀ آتش فشان های خاموش و نیمه فعال یافت می شود.
موارد استفاده سولفوریک اسید

مدل اتمی بور : نیلز بور فیزیکدان دانمارکی معتقد بود که الکترون ها در اطراف هستۀ اتم در سطوح انرژی (مدار) مشخصی قرار دارند. الکترون ها در در این مدارها به دور هسته در حال چرخش هستند.
طبق این مدل حداکثر تعداد الکترون هایی که در هر مدار می توانند باشند، از فرمول 2n2 به دست می آید که n شمارۀ مدار است.
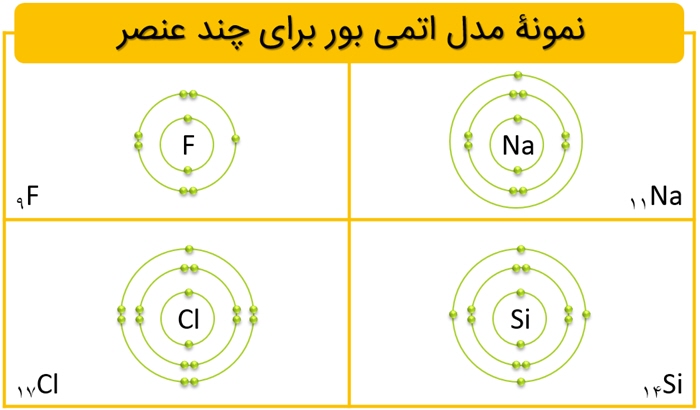

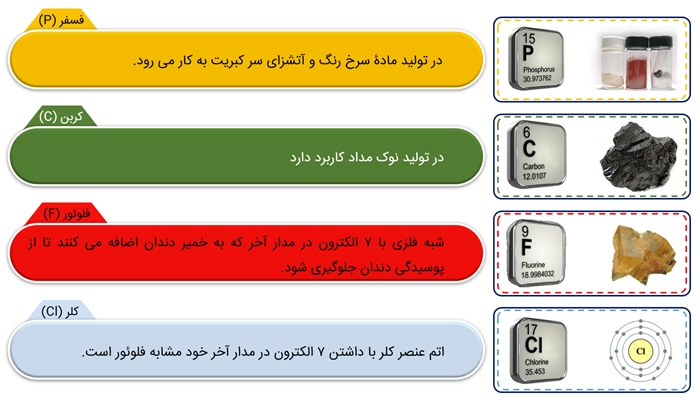
- کاربرد برخی نافلزات معروف

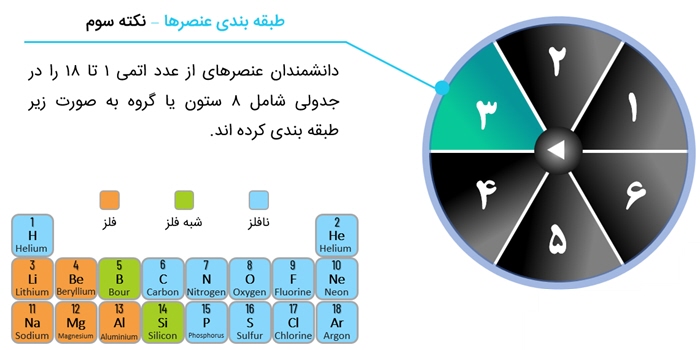
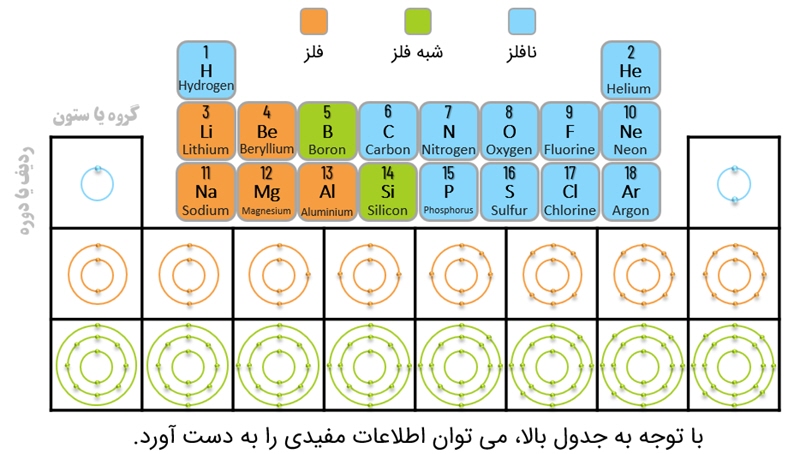
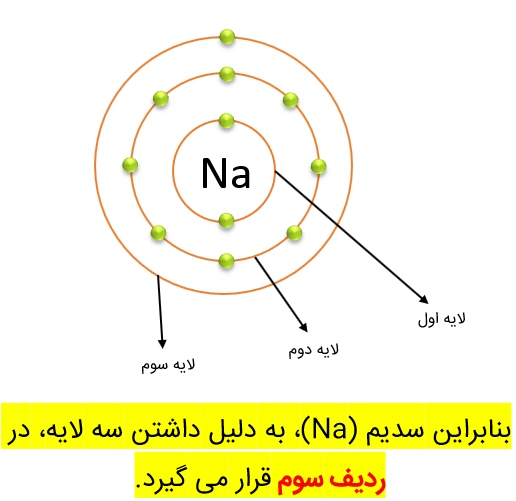
1. تعداد لایه ها نشان دهندۀ ردیفی است که عنصر در آن قرار دارد.
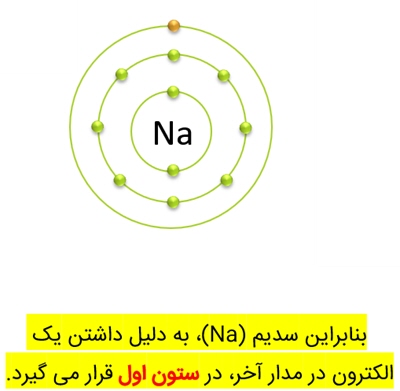
2. تعداد الکترون های لایۀ آخر، نشان دهندۀ ستونی از جدول است که عنصر در آن قرار دارد.
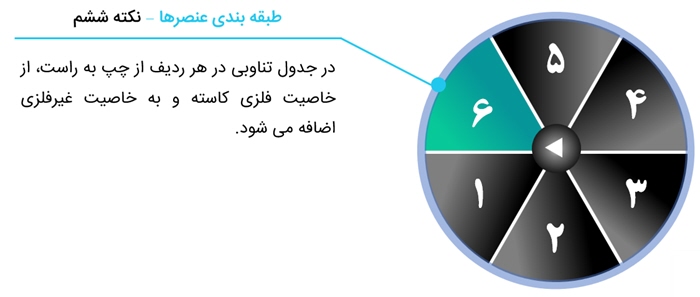
3. عناصری که در آخرین لایۀ خود 1 یا 2 یا 3 الکترون دارند، فلز و عناصری که در آخرین لایۀ خود 4 تا 8 الکترون دارند، نافلز هستند.

4. برخی از شبه فلزها در لایۀ آخر خود 3 یا 4 الکترون دارند.

5. عناصری که در یک گروه یا ستون قرار دارند، دارای ویژگی های مشترک زیادی هستند و بعضی از گروه ها اسامی اختصاصی نیز دارند. مانند :
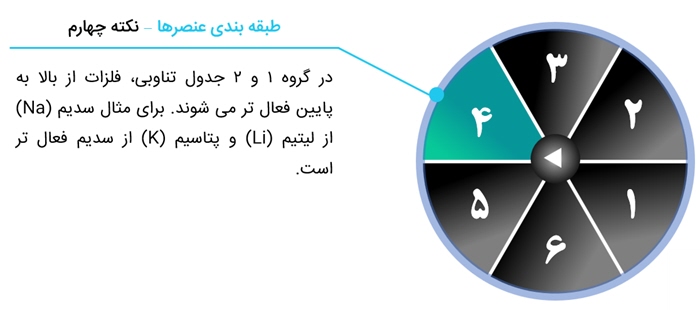
الف) فلزات قلیایی

این فلزات با آب به شدت واکنش می دهند و خاصیت قلیایی یا بازی ایجاد می کنند. |

فلزات نرمی هستند و با چاقو بریده می شوند. |

کاربردهای زیادی دارند مثلا لیتیم در باتری قابل شارژ استفاده می شود. |
ب) فلزات قلیایی خاکی
فلزات قلیایی خاکی نیز با آب واکنش می دهند و خاصیت بازی ایجاد می کنند. از آنجایی که داخل خاک زیاد پیدا می شوند؛ به فلزات قلیایی خاکی معروف هستند.

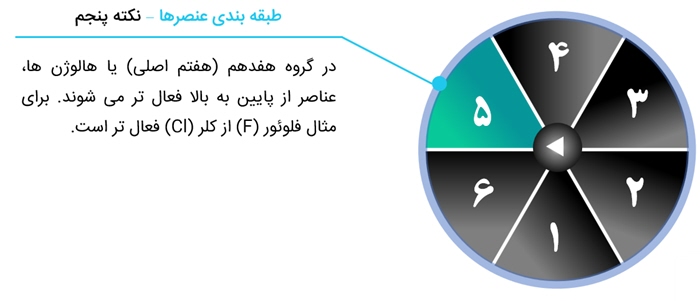
ج) هالوژن ها
نافلزهایی به شدت سمی هستند.
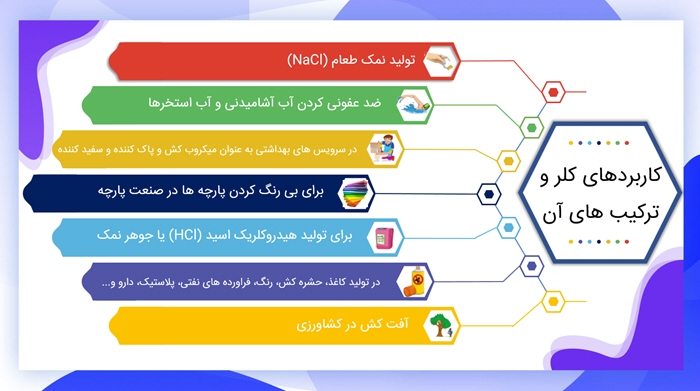
عنصر کلر که نمک را می سازد در این گروه قرار دارد. به همین دلیل به آنها نمک ساز یا هالوژن می گویند.

د) گازهای نجیب
گازهایی هستند که با مواد دیگر در حالت طبیعی واکنش نمی دهند، اما در شرایط سخت آزمایشگاهی امکان واکنش دارند.
گاز هلیم از این گروه است.















هیچ دیدگاهی نوشته نشده است.